6.1. Для углубленной идентификации, генетической паспортизации и определения клональности происхождения штаммов бруцелл используют метод MLVA, обладающий высокой дискриминирующей способностью, воспроизводимостью и достоверностью результатов.
Методика основана на сравнительном анализе локусных вариабельных тандемных повторов I и II хромосомы бруцелл и заключается в генотипировании штаммов Brucella spp. путем определения размера ампликона и количества тандемных повторов в VNTR-локусах.
С целью видовой идентификации применяется схема MLVA-8, включающая минисателлитные локусы Bruce 06, Bruce 08, Bruce 11, Bruce 12, Bruce 42, Bruce 43, Bruce 45, Bruce 5. Повышение числа исследуемых локусов придает большую достоверность филогенетическому и эпидемиологическому анализу, в связи с чем для определения клональности происхождения штаммов применяется схема MLVA-16, в которой к вышеописанным добавлены 8 микросателлитных локусов Bruce 04, Bruce 07, Bruce 09, Bruce 16, Bruce 18, Bruce 19, Bruce 21, Bruce 30 [18]. Учет результатов MLVA возможно осуществлять методом гель-электрофореза или микрокапиллярного электрофореза.
6.2. Для проведения реакции используют праймеры, представленные в табл. 25.
Праймеры для амплификации 16 VNTR-локусов Brucella spp.
|
Bruce 6 <*> |
||
|
Bruce 8 <*> |
||
|
Bruce 11 <*> |
||
|
Bruce 12 <*> |
||
|
Bruce 42 <*> |
||
|
Bruce 43 <*> |
||
|
Bruce 45 <*> |
||
|
Bruce 55 <*> |
||
Готовую смесь для ПЦР вносят по 10 мкл на дно пластиковых пробирок и добавляют 10 мкл выделенной ДНК. Затем пробирки помещают в амплификатор и проводят ПЦР в соответствии с режимом, приведенным в табл. 26.
Режим амплификации для MLVA-генотипирования
6.3. Учет результатов MLVA методом гель-электрофореза. Приготовление рабочих растворов и агарозного геля осуществляют в соответствии с инструкцией используемого комплекта реагентов для электрофоретической детекции продуктов амплификации в агарозном геле.
В лунки стандартного 3%-го агарозного геля вносят по 10 мкл ПЦР продуктов.
Электрофорез проводят при напряженности электрического поля 10 В/см, время устанавливается эмпирически. Для определения размера аллелей в первую и последнюю лунки геля вносят маркер длин ДНК или ампликоны штаммов возбудителя бруцеллеза, размеры которых ранее определены методом прямого секвенирования.
По окончании электрофореза гель помещают на стекло трансиллюминатора, обрабатывают изображение с помощью программного обеспечения для гель-документирования в соответствии с инструкцией и определяют размеры полученных ампликонов по всем локусам для каждого исследуемого штамма (рис. 9).
Рис. 9. Электрофореграмма продуктов амплификации локуса
Brace 30 штаммов B. abortus: М - маркер молекулярных масс
(100, 200, 300, 500, 700, 1000 п.н.),
Р - аллельный маркер (142 п.н.)
6.4. Учет результатов MLVA методом микрокапиллярного электрофореза. Приготовление рабочих растворов и подготовку чипа осуществляют в соответствии с инструкцией используемого комплекта реагентов. В качестве маркера длин ДНК используют коммерческий стандарт из набора реагентов для электрофореза.
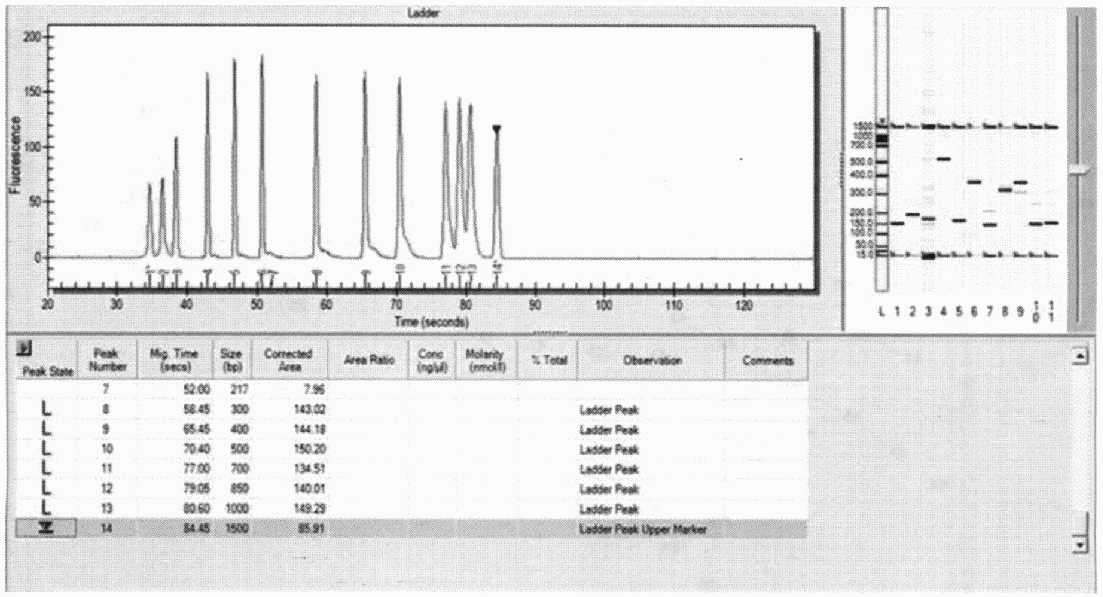
Разделение фрагментов амплификации и определение размеров полученных ампликонов осуществляется программой прибора автоматически (рис. 10).
Рис. 10. Электрофореграмма продуктов амплификации
возбудителя бруцеллеза, полученная с помощью станции
микрокапиллярного электрофореза по результатам MLVA-16
6.5. Перевод размеров локусов, полученных в парах нуклеотидов, в число тандемных повторов по каждому из локусов проводится по следующим формулам (где N - длина полученного ампликона, п.н., n - число тандемных повторов) (1):
6.6. Полученные данные сравнивают с существующими базами данных по MLVA-генотипам штаммов Brucella spp.
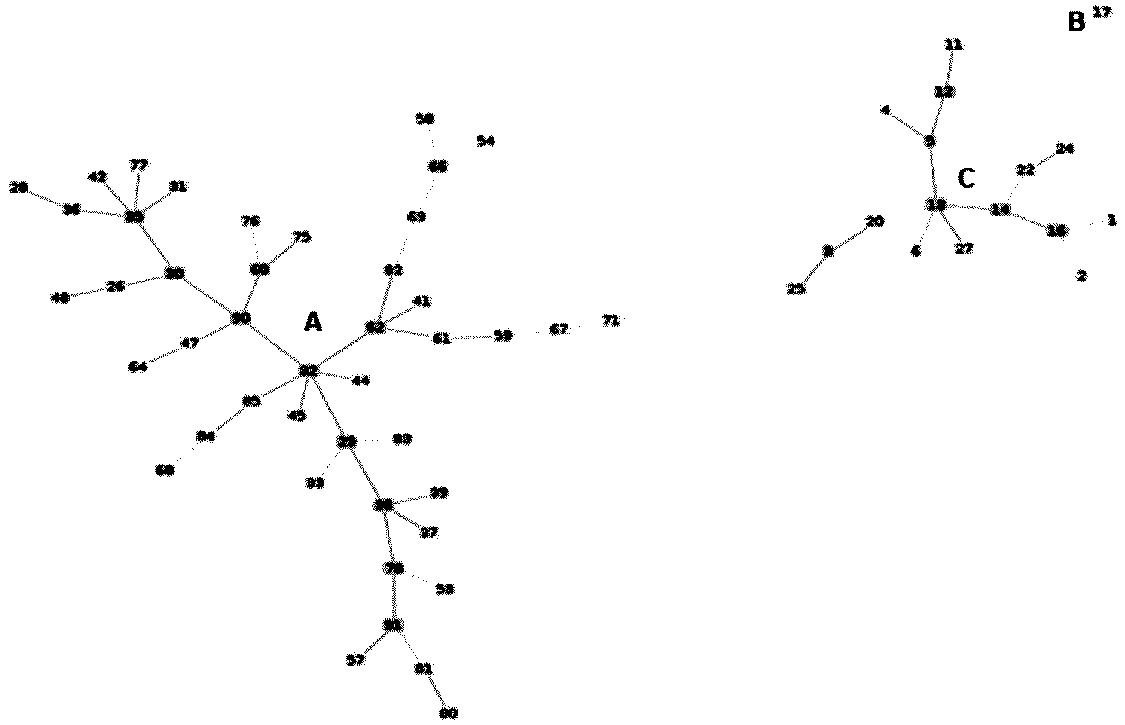
Определение степени генетического родства между изолятами проводят с помощью филогенетического анализа, который отображен графически (рис. 11) в виде дендрограммы (филогенетического дерева).
Рис. 11. Дендрограмма штаммов Brucella spp.
по результатам MLVA-16
- Гражданский кодекс (ГК РФ)
- Жилищный кодекс (ЖК РФ)
- Налоговый кодекс (НК РФ)
- Трудовой кодекс (ТК РФ)
- Уголовный кодекс (УК РФ)
- Бюджетный кодекс (БК РФ)
- Арбитражный процессуальный кодекс
- Конституция РФ
- Земельный кодекс (ЗК РФ)
- Лесной кодекс (ЛК РФ)
- Семейный кодекс (СК РФ)
- Уголовно-исполнительный кодекс
- Уголовно-процессуальный кодекс
- Производственный календарь на 2025 год
- МРОТ 2026
- ФЗ «О банкротстве»
- О защите прав потребителей (ЗОЗПП)
- Об исполнительном производстве
- О персональных данных
- О налогах на имущество физических лиц
- О средствах массовой информации
- Производственный календарь на 2026 год
- Федеральный закон "О полиции" N 3-ФЗ
- Расходы организации ПБУ 10/99
- Минимальный размер оплаты труда (МРОТ)
- Календарь бухгалтера на 2026 год
- Частичная мобилизация: обзор новостей
- Постановление Правительства РФ N 1875

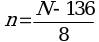 ;
;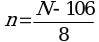 ;
;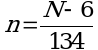 ;
;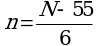 ;
;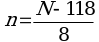 ;
;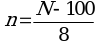 ;
;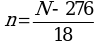 ;
;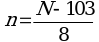 ;
;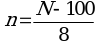 ;
;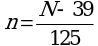 ;
;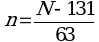 ;
;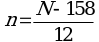 ;
;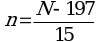 ;
;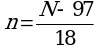 ;
;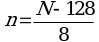 ;
;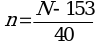 .
.